Ο ΔΡ. Σταύρος Π. Δερδας, MD, MSC, PHD Μοριακός Ογκολόγος εξηγεί:

Η ραγδαία εξέλιξη της μοριακής βιολογίας και της γονιδιωματικής ανάλυσης τα τελευταία χρόνια έχει μεταμορφώσει τον τρόπο με τον οποίο προσεγγίζουμε τη διάγνωση και τη θεραπεία του καρκίνου. Ανάμεσα στα πιο καινοτόμα εργαλεία αυτής της νέας εποχής βρίσκεται η υγρή βιοψία (liquid biopsy), μια μη επεμβατική τεχνική που επιτρέπει την ανίχνευση και παρακολούθηση του καρκίνου μέσω της ανάλυσης δειγμάτων αίματος ή άλλων σωματικών υγρών.
Η υγρή βιοψία υπόσχεται να φέρει μια επανάσταση στην ογκολογία, παρέχοντας τη δυνατότητα για έγκαιρη διάγνωση, συνεχή παρακολούθηση της νόσου, αξιολόγηση της ανταπόκρισης στη θεραπεία και ανίχνευση υποτροπών — όλα με ένα απλό δείγμα αίματος.
Τι είναι η υγρή βιοψία
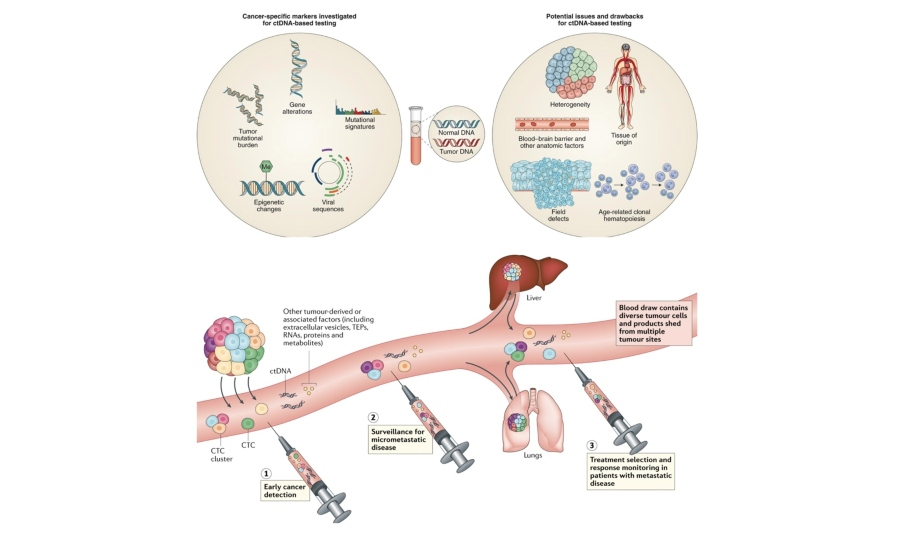
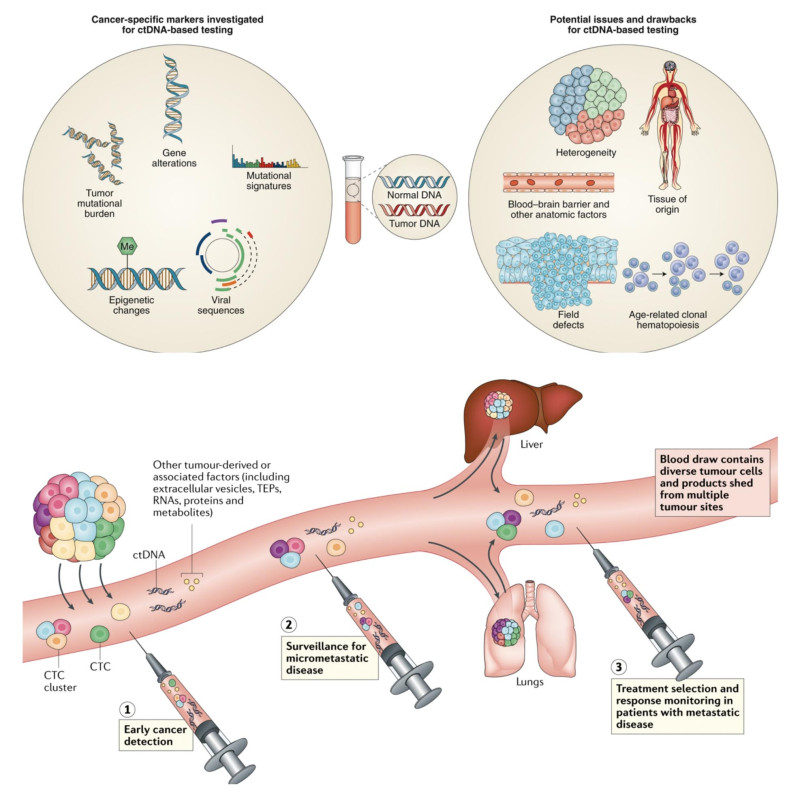
Σε αντίθεση με τη συμβατική βιοψία, που απαιτεί τη λήψη ιστού μέσω επεμβατικής διαδικασίας, η υγρή βιοψία βασίζεται στην ανίχνευση βιοδεικτών που κυκλοφορούν στα σωματικά υγρά. Οι σημαντικότεροι από αυτούς περιλαμβάνουν:
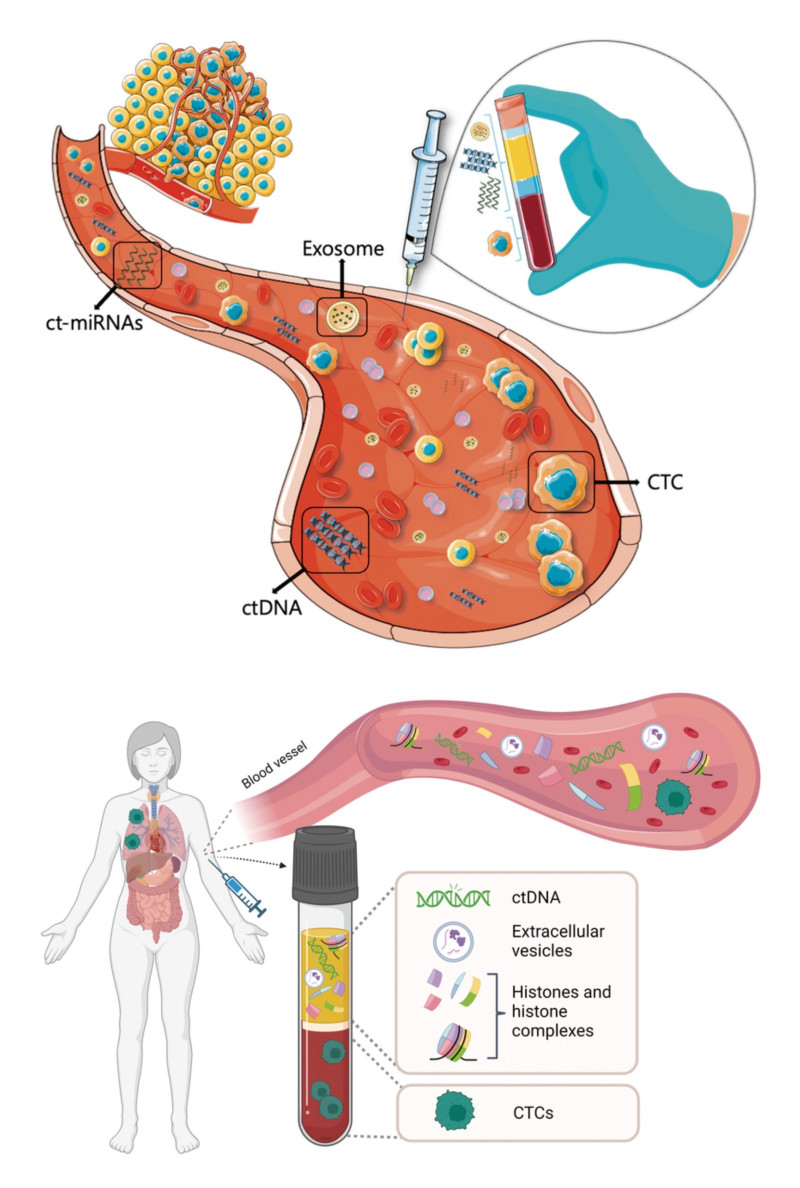
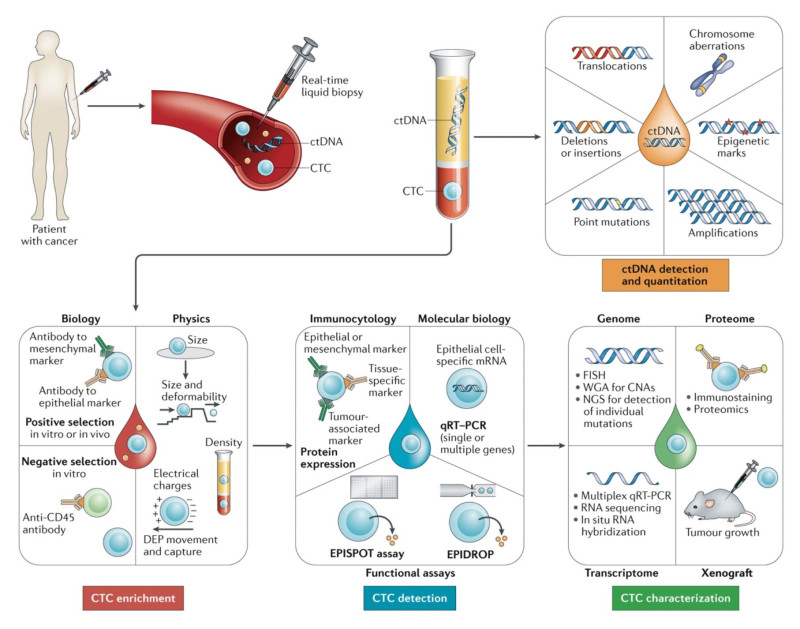
- Κυκλοφορούν DNA όγκου (ctDNA - circulating tumor DNA): μικρά θραύσματα DNA που απελευθερώνονται από τα καρκινικά κύτταρα στο αίμα.
- Κυκλοφορούντα καρκινικά κύτταρα (CTCs - circulating tumor cells): ολόκληρα κύτταρα που αποκολλώνται από τον πρωτοπαθή όγκο και εισέρχονται στην κυκλοφορία.
- Εξωσώματα και μικροσωματίδια που περιέχουν πρωτεΐνες, RNA και άλλα μόρια με πληροφορίες για τον όγκο.
Η ανάλυση αυτών των στοιχείων μπορεί να αποκαλύψει γονιδιακές μεταλλάξεις, επιγενετικές αλλαγές ή δείκτες ανθεκτικότητας στη θεραπεία, προσφέροντας μια δυναμική και σε πραγματικό χρόνο εικόνα της νόσου.
Πλεονεκτήματα σε σχέση με την παραδοσιακή βιοψία
Η υγρή βιοψία υπερτερεί της κλασικής ιστικής βιοψίας σε πολλαπλά επίπεδα:
1. Μη επεμβατική: Δεν απαιτεί χειρουργική παρέμβαση ή αναισθησία, μειώνοντας τον κίνδυνο και το κόστος.
2. Δυνατότητα επαναληψιμότητας: Μπορεί να πραγματοποιείται συχνά, επιτρέποντας συνεχή παρακολούθηση της εξέλιξης του όγκου και της ανταπόκρισης στη θεραπεία.
3. Ανίχνευση ετερογένειας: Οι όγκοι είναι ετερογενείς· η ανάλυση αίματος αντικατοπτρίζει μεταλλάξεις από διαφορετικές περιοχές του όγκου ή και μεταστάσεις.
4. Πρόβλεψη υποτροπής: Μπορεί να εντοπίσει υπολειπόμενη νόσο (minimal residual disease, MRD) πριν γίνει κλινικά ανιχνεύσιμη.
Χάρη σε αυτά τα πλεονεκτήματα, η υγρή βιοψία θεωρείται το «μέλλον» της ογκολογικής παρακολούθησης, ιδιαίτερα για ασθενείς που δεν μπορούν να υποβληθούν σε νέα ιστική βιοψία ή για παρακολούθηση της νόσου σε πραγματικό χρόνο.
Τεχνολογίες ανάλυσης και ανίχνευσης
Η επιτυχία της υγρής βιοψίας βασίζεται στις εξελιγμένες τεχνολογίες μοριακής ανάλυσης που μπορούν να ανιχνεύσουν ελάχιστες ποσότητες καρκινικού DNA στο αίμα. Οι κύριες τεχνικές περιλαμβάνουν:
- PCR υψηλής ευαισθησίας (digital PCR, BEAMing): Επιτρέπει την ανίχνευση γνωστών μεταλλάξεων με εξαιρετική ακρίβεια.
- NGS (Next-Generation Sequencing): Επιτρέπει την ταυτόχρονη ανάλυση πολλών γονιδίων και τον εντοπισμό νέων μεταλλάξεων χωρίς προϋπάρχουσα γνώση.
Epigenetic assays για την ανίχνευση μεταβολών μεθυλίωσης DNA, που προσφέρουν υψηλή ειδικότητα για ορισμένους τύπους καρκίνου.
Ο συνδυασμός αυτών των τεχνικών καθιστά δυνατή τη χαρτογράφηση του μοριακού προφίλ του όγκου με τρόπο δυναμικό και προσαρμοσμένο στον κάθε ασθενή.
Κλινικές εφαρμογές
Η υγρή βιοψία έχει ήδη βρει εφαρμογές σε διάφορους τομείς της ογκολογίας:
1. Έγκαιρη διάγνωση
Η ανίχνευση ctDNA μπορεί να αποκαλύψει την παρουσία καρκίνου πολύ πριν από την εμφάνιση συμπτωμάτων ή ευρημάτων σε απεικονιστικές εξετάσεις. Έρευνες δείχνουν ότι ορισμένες μεταλλάξεις στο ctDNA μπορούν να προβλέψουν την ανάπτυξη καρκίνου μήνες ή και χρόνια πριν τη διάγνωση.
2. Επιλογή θεραπείας
Μέσω της ανίχνευσης συγκεκριμένων μεταλλάξεων (π.χ. EGFR, KRAS, BRAF), οι γιατροί μπορούν να επιλέξουν στοχευμένες θεραπείες χωρίς να απαιτείται νέα ιστική βιοψία.
3. Παρακολούθηση
ανταπόκρισης
Η ποσοτική μεταβολή του ctDNA κατά τη διάρκεια της θεραπείας παρέχει μια άμεση ένδειξη για την αποτελεσματικότητά της, συχνά πριν γίνουν ορατές αλλαγές στην απεικόνιση.
4. Ανίχνευση υποτροπής
Μετά την ολοκλήρωση της θεραπείας, η υγρή βιοψία μπορεί να ανιχνεύσει ελάχιστη υπολειπόμενη νόσο, επιτρέποντας την έγκαιρη παρέμβαση πριν την κλινική υποτροπή.
Περιορισμοί και προκλήσεις
Παρά την εντυπωσιακή πρόοδο, η υγρή βιοψία δεν έχει αντικαταστήσει ακόμη την ιστική βιοψία. Ορισμένοι περιορισμοί περιλαμβάνουν:
- Χαμηλή συγκέντρωση ctDNA σε πρώιμα στάδια καρκίνου, που μπορεί να δυσκολεύει την ανίχνευση.
- Απουσία τυποποιημένων πρωτοκόλλων για τη συλλογή, αποθήκευση και ανάλυση δειγμάτων.
- Ψευδώς αρνητικά αποτελέσματα, όταν ο όγκος δεν απελευθερώνει επαρκές DNA στο αίμα.
- Κόστος και ανάγκη εξειδικευμένου εξοπλισμού σε ορισμένες τεχνικές υψηλής ευαισθησίας.
Ωστόσο, με τη συνεχή εξέλιξη των τεχνολογιών και τη μείωση του κόστους αλληλούχισης, αυτά τα εμπόδια σταδιακά ξεπερνιούνται.
Το μέλλον της υγρής βιοψίας
Η υγρή βιοψία αναμένεται να διαδραματίσει κεντρικό ρόλο στη διάγνωση και διαχείριση του καρκίνου στο μέλλον. Ήδη βρίσκονται σε εξέλιξη πολυκεντρικές μελέτες για την ενσωμάτωσή της σε προγράμματα πληθυσμιακού ελέγχου (screening), ενώ ερευνάται και η χρήση της σε μη ογκολογικές παθήσεις, όπως φλεγμονώδεις ή νευροεκφυλιστικές νόσοι.
Η συνδυαστική ανάλυση διαφορετικών τύπων βιοδεικτών (ctDNA, RNA, πρωτεϊνών, εξωσωμάτων) και η αξιοποίηση τεχνητής νοημοσύνης για την ερμηνεία των δεδομένων ανοίγουν νέους ορίζοντες στην προσωποποιημένη ιατρική.
Η υγρή βιοψία δεν είναι πλέον μια πειραματική τεχνική· είναι ένα εργαλείο που αλλάζει τον τρόπο με τον οποίο αντιλαμβανόμαστε την ογκολογική φροντίδα - από τη στατική διάγνωση, στη δυναμική και συνεχή παρακολούθηση της νόσου.
Συμπέρασμα
Η υγρή βιοψία αντιπροσωπεύει μια ουσιαστική αλλαγή παραδείγματος στη διάγνωση και θεραπευτική παρακολούθηση του καρκίνου. Με τη δυνατότητα να προσφέρει ακριβή, γρήγορα και επαναλήψιμα αποτελέσματα, δίνει στους ιατρούς ένα πολύτιμο εργαλείο για τη λήψη κλινικών αποφάσεων και στους ασθενείς ελπίδα για πιο στοχευμένες και λιγότερο επεμβατικές θεραπείες.
Καθώς η τεχνολογία προχωρά και οι γνώσεις μας για το μικροπεριβάλλον του όγκου βαθαίνουν, η υγρή βιοψία έχει τη δυναμική να μετατραπεί από ερευνητικό εργαλείο σε καθιερωμένη κλινική πρακτική, ανοίγοντας τον δρόμο προς μια νέα εποχή προσωποποιημένης ιατρικής ακρίβειας.
Πηγή Τίτλος / Σύντομη Περιγραφή
Ma L, et al. Liquid biopsy in cancer: current status, challenges and future perspectives - μια πρόσφατη ανασκόπηση που καλύπτει τεχνικές, περιορισμούς και προοπτικές (Nature)
Nikanjam M, et al. Liquid biopsy: current technology and clinical applications - συνοπτική παρουσίαση τεχνολογιών όπως ddPCR, BEAMing, NGS και των κλινικών εφαρμογών (BioMed Central)
Connal S, et al. Liquid biopsies: the future of cancer early detection - εστίαση στην πρώιμη διάγνωση, τα πλεονεκτήματα και τις προκλήσεις (PMC)
Michela B, et al. Liquid Biopsy: A Family of Possible Diagnostic Tools - ανάλυση διαφορετικών τύπων υγρής βιοψίας πέραν του αίματος, όπως ούρα, σάλιο κ.ά. (MDPI)
Liu SC, et al. Circulating tumor DNA in liquid biopsy: Current diagnostic challenges - εντοπίζει περιορισμούς, ανοίγοντας δρόμους βελτίωσης (wjgnet.com)
Zhang S, et al. Tracing the history of clinical practice of liquid biopsy - μελέτη βιβλιομετρίας που δείχνει την εξέλιξη και τη διάδοση της υγρής βιοψίας στον χρόνο (Frontiers)
Dive C Η Caroline Dive είναι μία από τις κορυφαίες ερευνήτριες στη χρήση των CTCs και του ctDNA ως εργαλεία διάγνωσης και παρακολούθησης καρκίνου (Wikipedia)
Sarah-Jane Dawson Ειδικεύεται στην ανάπτυξη μη επεμβατικών βιοδεικτών (liquid biopsy) για κλινική χρήση, ειδικά στην ογκολογία (Wikipedia)